Lai arī pasaulē uzlabojas onkoloģijas pacientu diagnostika un to ārstniecības iespējas, tomēr mirstība no audzējiem aizvien ir augsta. Tas ir saistīts ar audzēja rezistenci jeb tā spēju sekmīgi pretoties dažādām terapijām. Kā skaidro šūnu bioloģe, LU KRMI pētniece un LU fonda pārvaldītā projekta “Rezistences rašanās audzēju terapijas rezultātā” vadītāja Zane Simsone, pielietotā terapija ne vienmēr ir veiksmīga tādēļ, ka pastāv audzēja heterogenitāte, vēža šūnu polimorfisms un dažāda šūnu funkcionālā aktivitāte vienos un tajos pašos vēža audos. Proti, vēža šūnas ir neviendabīgas, turklāt to vidū sastopamas ģenētiski atšķirīgas formas.
LU KRMI pētnieku grupas iegūtie jaunākie dati un rezultāti palīdzēs detalizēti raksturot mikrošūnas un uzzināt, kurā brīdī tās rodas, kad tās spēj uzņemt visvairāk vielu, turklāt pētnieki sniegs iespēju izzināt citas mikrošūnām raksturīgās īpatnības. Šāds pētījums ļaus nākotnē izprast, kāpēc audzēja terapija ne vienmēr ir veiksmīga. Turklāt iegūtās zināšanas varētu izmantot, lai novērtētu pretvēža terapijas efektivitāti, bet tālākā nākotnē varētu izstrādāt pretvēža medikamentus. Projektu atbalsta Latvijas Universitātes platīna mecenāts “Mikrotīkls” sadarbībā ar Latvijas Universitātes fondu.
Mikrošūnas – drauds sekmīgai audzēja terapijai
Pētījumos visā pasaulē tiek uzskatīts, ka vēža cilmes šūnas ir rezistentas pret pielietoto pretvēža terapiju. Praksē plaši izmantotā ķīmijterapija un staru terapija rada DNS bojājumus, neļaujot audzēja šūnām dalīties un veicinot to bojāeju. Kaut arī vēža cilmes šūnas tiek saistītas ar terapijas zemo efektivitāti, par tām tiek runāts kā par heterogēna audzēja subpopulāciju. Līdz šim veiktajos pētījumos novērots, ka vēža cilmes šūnām piemīt DNS atjaunošanas mehānismi, tādējādi spējot izvairīties no medikamentu ietekmes un iedarbības. Par vēža cilmes šūnām pastāv vairākas hipotēzes, un tajās parādās šādas galvenās vēža cilmes šūnu iezīmes:
- tikai nelielam daudzumam audzēja šūnu piemīt tumorogēnisks (audzēju veidojošs) potenciāls;
- vēža cilmes šūnu populāciju var nodalīt no pārējām vēža šūnām, izmantojot to virsmu marķierus;
- vēža cilmes šūnu populācijai piemīt pašatjaunošanās un proliferācijas iespējas.
Vēža cilmes šūnas netiek apskatītas pēc pielietotās terapijas, respektīvi, netiek raksturotas pretvēža terapijas rezistentās šūnas un to īpašības. Latvijā pētījumus par šūnu izmaiņām un veidošanos, apskatot audzēja šūnu līnijas pretvēža terapijas ietekmē, pēta vairāki zinātnieki. Patlaban vienīgais zinātnieks, kurš pēta mikrošūnas, ir bioloģijas doktors, zinātnieks Indulis Buiķis ar kolēģiem. Pētniecības grupa novērojusi maza izmēra šūnas – mikrošūnas. Tās ir apaļas vai ovālas šūnas ar nelielu citoplazmu (šūnu daļas, kas aptver kodolu). Mikrošūnas tiek raksturotas kā dabīgas audzēja komponentes, un to skaits pielietotās pretvēža terapijas ietekmē pieaug, proti, mikrošūnas tiek uzskatītas par potenciālām audzēja atjaunojošajām šūnām pēc paša audzēja bojāejas. Pirmie rezultāti liecina, ka mikrošūnās notiek intensīvi bioķīmiski procesi. Šādas mikrošūnas ir novērotas, piemēram, Džungārijas kāmja un cilvēka sarkomas jeb ļaundabīga saistaudu audzēja HT-1080 šūnu līnijās pēc šūnu apstrādes ar pretvēža zālēm, metanolu, hipertermiski apstrādājot šūnas un audzējot šūnas nepietiekamā barotnē.
Mikrošūnu veidošanās tiek skaidrota ar sporozes procesu, kad pretvēža terapijas ietekmē no letāli bojātām vēža šūnām atsevišķos gadījumos var attīstīties jaunas šūnas ar cilmes šūnām līdzīgām īpašībām, kā rezultātā no bojātas vēža šūnas veidojas viena vai vairākas mikrošūnas.
1.  2.
2. 
3.  4.
4. 
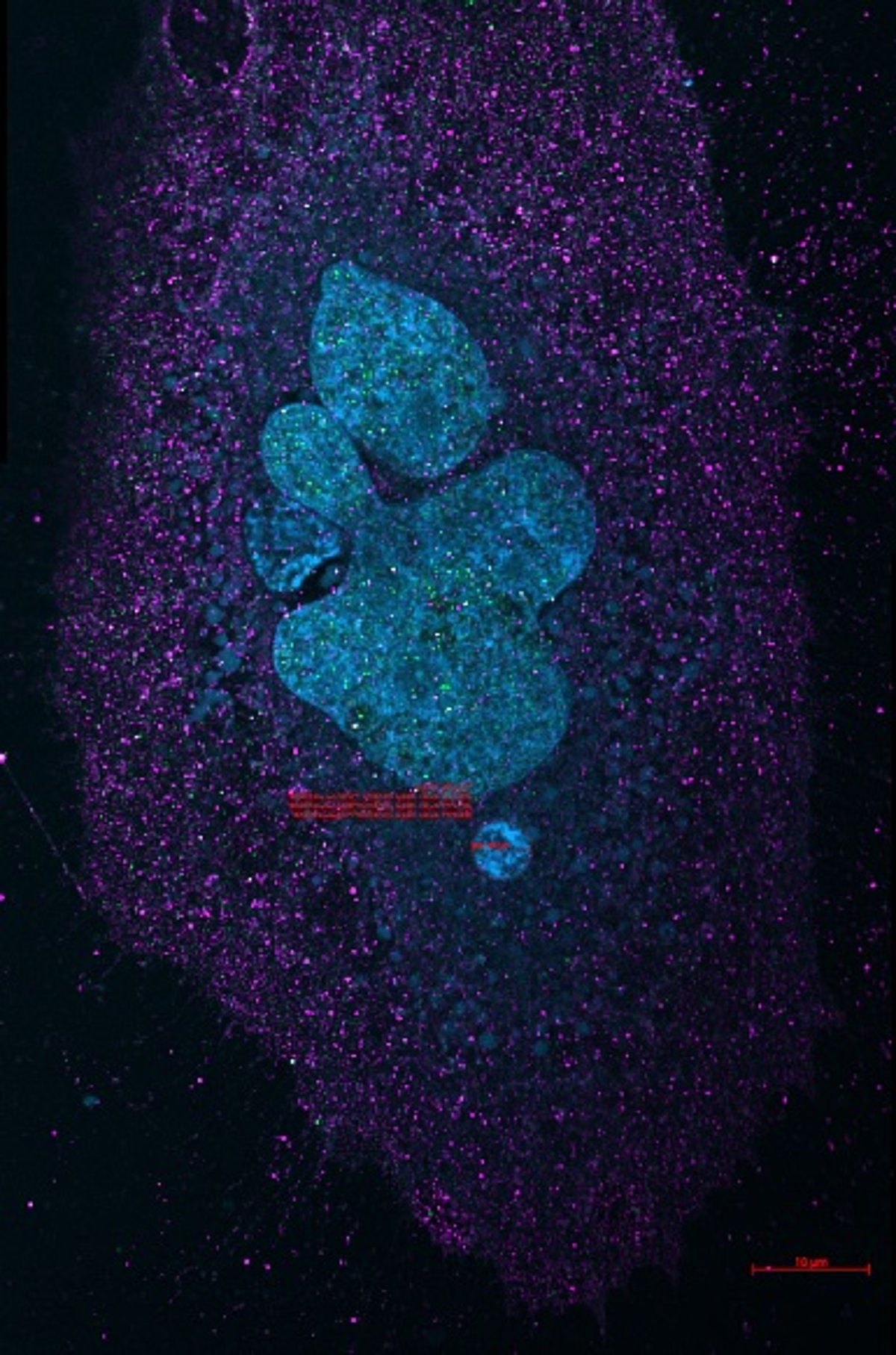
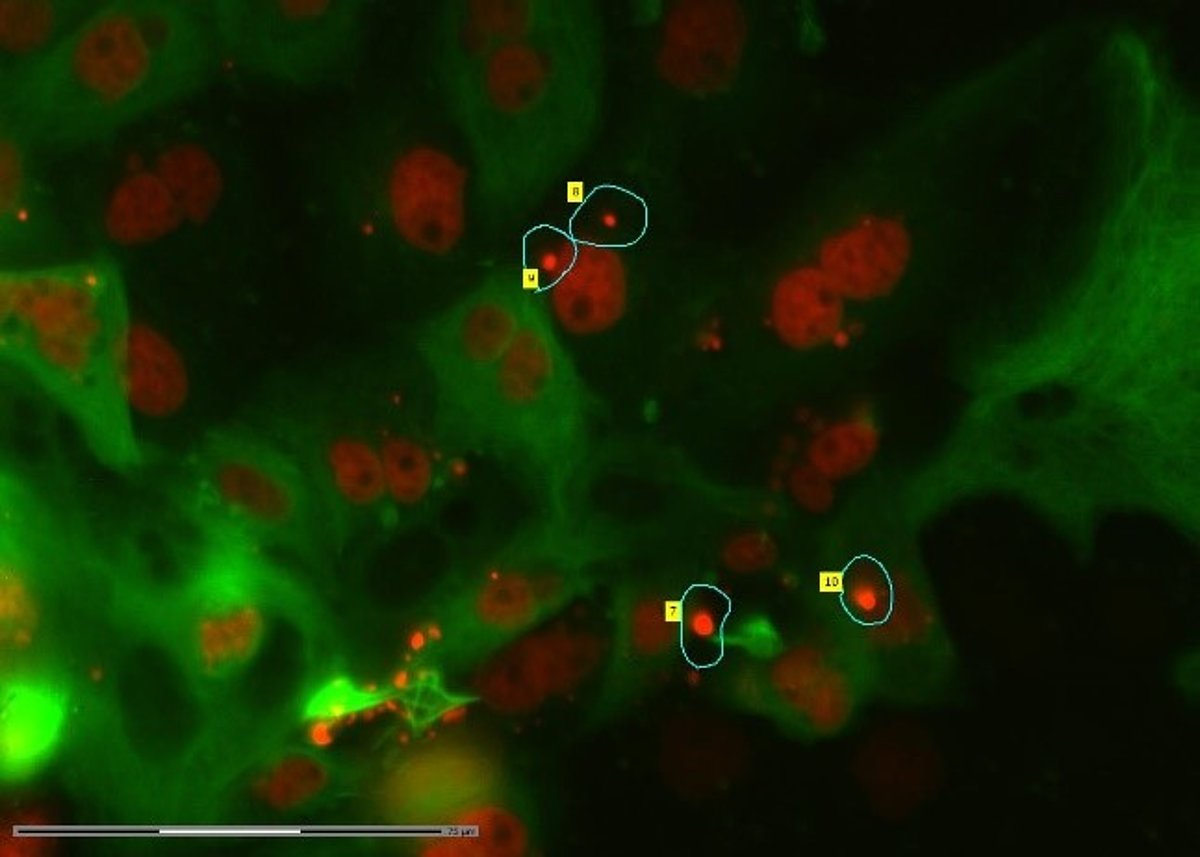
1. Cūkas nieres šūnu līnijas LLCPK1 kontroles šūnas. Zaļš – citoplazma, sarkans – kodols. 2. Cūkas nieres šūnu līnijas LLCPK1 ar pretvēža aģentu apstrādātas šūnas. Zaļš – citoplazma, sarkans – kodols. 3. Cūkas nieres šūnu līnijas LLCPK1 ar pretvēža aģentu apstrādātas šūnas. Šūnu grupas iezīmēšana mikrodisekcijai. 4. Cūkas nieres šūnu līnijas LLCPK1 ar pretvēža aģentu apstrādātas šūnas. Vienas šūnas iezīmēšana mikrodisekcijai.
Attēlu iegūšana un šūnu izolēšana veikta ar Laser Microdissection with ZEISS PALM MicroBeam. Autore – Zane Simsone.
Vizuālā kontrole rada pozitīvu pavērsienu audzēju terapijas uzlabošanā
Patlaban noteiktās mikrošūnu raksturojošās pazīmes – to mazais izmērs un endocitozes (spēja uzņemt šūnā citas apkārt esošās vielas) īpašības. Tieši endocitozes īpašība, kas piemīt mikrošūnām, ir to atšķirība no vēža cilmes šūnām. Tādēļ ir svarīgi veikt pētījumus par terapijai rezistentām šūnām, nosakot to funkcionālās īpašības un mikrošūnu raksturojošos marķierus. Šobrīd mikrošūnu identificēšana pēc pielietotās terapijas notiek, morfoloģiski izmantojot mikroskopiju, imūncitoķīmiskās identificēšanas metodes un plūsmas citometriju, iedalot šūnas pēc to lieluma un ekspresējošiem marķieriem. Plūsmas citometrijas izmantošanai ir gan priekšrocības, gan trūkumi. Pozitīvās īpašības – var izanalizēt lielāku šūnu skaitu. Tomēr par negatīvu aspektu uzskatāms tas, ka mikrošūnu aizmetņi ir mazāki par 1,5 mikrometriem. Izmantojot standarta plūsmas citometrijas metodi, šādi paraugi tiek iedalīti zem uztveršanas sliekšņa kā artefakti. Tādējādi vienas šūnas analīzei būtu svarīga vizuālā kontrole, un šādu iespēju sniedz mikrodisekcijas iekārta. Izmantojot šo iekārtu, ir iespējams iegūt pētnieku grupai interesējošās šūnas tālākai analīzei no šūnu kultūrām, saldētu audu paraugu griezumiem un formalīnā fiksētiem parafīnā ieguldītiem audu griezumiem.
Ja interesējošās šūnas ir izdalītas no šūnu kultūras, tad ir iespējama izolēto šūnu tālāka kultivēšana, lai novērtētu to dzīvotspēju. Šajā vasarā sadarbībā ar ZEISS mikroskopijas centru Oberkohenā, Vācijā, projekta vadītāja Zane Simsone ar bioloģijas doktoru Tālivaldi Freivaldu un citiem kolēģiem no LU KRMI veica piloteksperimentu ar mikrošūnu izdalīšanu pēc apstrādes ar pretvēža līdzekli un to ataudzēšanu. Projekta laikā tika izmantotas divas šūnu līnijas – cilvēka osteosarkomas (ļaundabīgs kaulu audzējs) un cūkas nieru šūnu līnijas. Šūnas tika apstrādātas ar pretvēža aģentu un pēc divām diennaktīm, izmantojot mikrodisekcijas iekārtu, tika izdalītas dažādu šūnu subpopulācijas, tai skaitā mikrošūnas. Izdalītās šūnas tālāk kultivētas līdz septītajai dienai, uzņemot fotoattēlu katru otro dienu. Pētnieku grupa turpina analizēt iegūtos datus, bet jau šī brīža rezultāti liecina, ka šo metodi var pielietot, lai izolētu interesējošo šūnu vai šūnu grupu, to nebojājot.
Konferences tēzes (145. lpp.) no EPMA Pasaules kongresa 2019, Pilzenē, Čehijā >>
EPMA - (Eiropas Paredzamo, profilaktisko un personalizēto zāļu asociācija) European Association for Predictive Preventive & Personalised Medicine.
Par Latvijas Universitātes fondu
Jau kopš 2004. gada Latvijas Universitātes fonds nodrošina iespēju mecenātiem un sadarbības partneriem atbalstīt gan LU, gan citas vadošās Latvijas augstskolas, tā investējot Latvijas nākotnē. LU fonda prioritātes ir atbalstīt izcilākos studentus un pētniekus, veicināt modernas mācību vides izveidi, kā arī universitātes ēku būvi un rekonstrukciju.

 Akadēmiskais centrs
Akadēmiskais centrs